Come somministrare i monoclonali EV e sottocute. Le indicazioni per gli infermieri
L'Organizzazione mondiale della sanità ha preparato una infografica che riassume con immagini le informazioni per la somministrazione dell'associazione casirivimab-imdevimab contro COVID-19 - WHO_istruzioni_somministrazione_casirivimab-e-imdevimab
I due anticorpi sono attivi contro le varianti Alfa, Beta, Gamma e Delta, mentre evidenze emergenti prevedono una diminuzione dell'efficacia contro Omicron, si legge in avvio del documento.
Per chi sono indicati casirivimab e imdevimab?
- Per i pazienti con COVID-19 confermato non grave, ma a rischio di progressione della malattia e di ospedalizzazione.
- Coloro che sono a più alto rischio in generale:
- hanno età avanzata
- presentano immunodeficienza e malattie croniche
- non sono vaccinati.
- Per i pazienti con confermata sieronegatività grave o critica a SARS-CoV-2. I test sierologici dovrebbero rilevare la presenza degli anticorpi della proteina spike di SARS-CoV-2.
I fattori di rischio comprendono anche:
- età superiore a 60 anni, ipertensione, diabete, malattie cardiache, malattie polmonari croniche o cerebrovascolari, demenza, disturbi mentali, malattie renali croniche, immunosoppressione (incluso HIV), obesità e cancro
- gravidanza, età materna avanzata, indice di massa corporea elevato e condizioni croniche pregresse
Esistono dati limitati sull'uso di casirivimab e imdevimab in donne in gravidanza con COVID-19. In questi casi, la decisione sull'uso della terapia dovrà essere effettuata in consultazione tra medico e paziente.
Le controindicazioni a casirivimab e imdevimab includono individui di ≥ 12 anni, ≥ 40 kg o allergici a un componente della terapia.
DOSAGGIO
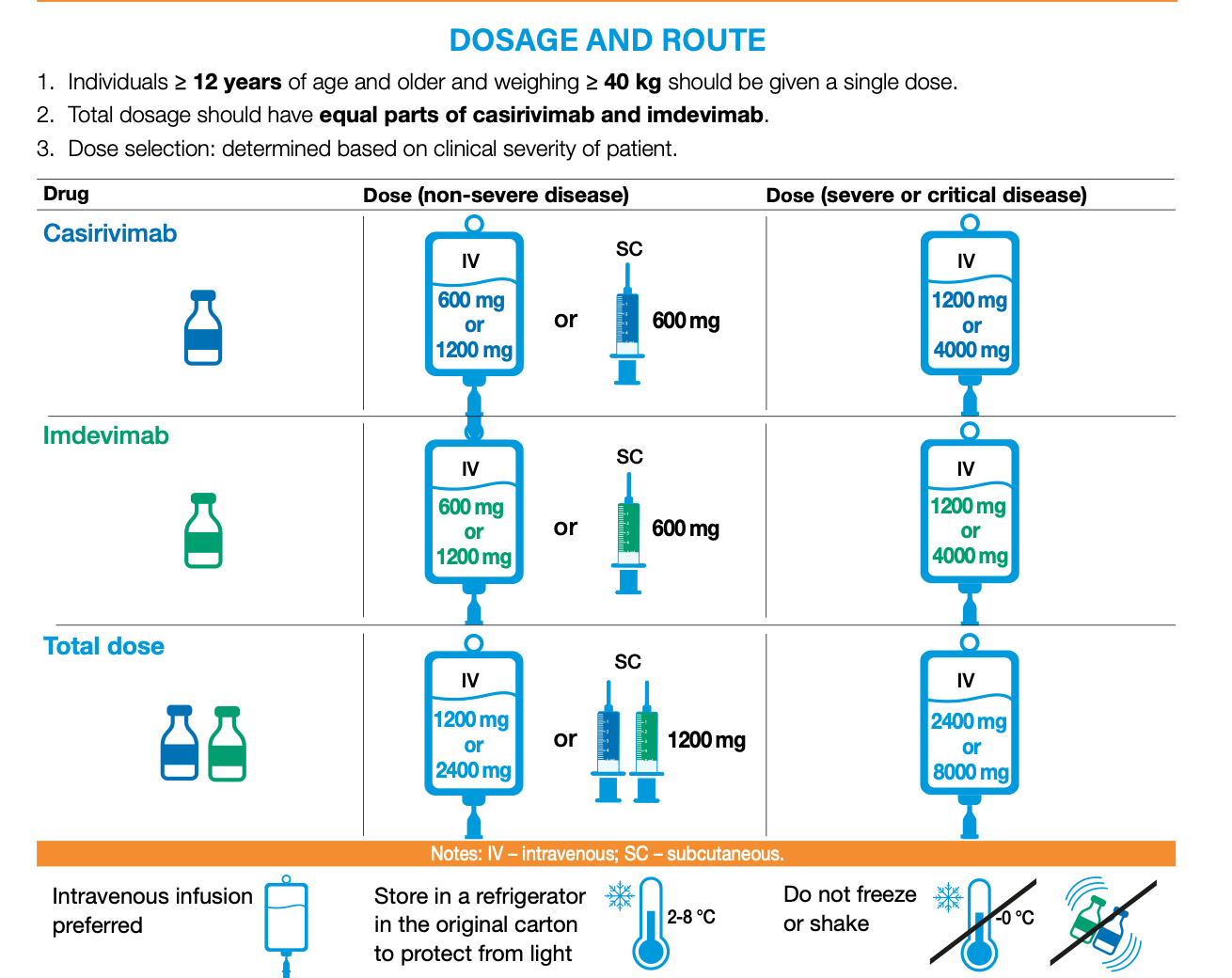
- Ai soggetti di età ≥ 12 anni e più e di peso ≥ 40 kg deve essere somministrata una dose singola. Il dosaggio totale dovrebbe avere parti uguali di casirivimab e imdevimab.
- Selezione della dose: determinata in base alla gravità clinica del paziente.
PREPARAZIONE
Istruzioni operative
- Estrarre i flaconcini di casirivimab e imdevimab dal frigorifero (2-8 °C) e attendere circa 20 minuti affincheÌ raggiungano la temperatura ambiente prima della preparazione. Non esporre al calore diretto. Non agitare i flaconcini
- Prima della somministrazione, ispezionare visivamente i flaconcini di casirivimab e imdevimab per escludere la presenza di particolato o alterazione del colore. Se si osserva particolato o alterazione del colore, scartare i concentrati e utilizzare flaconcini nuovi. I concentrati presenti in ciascun flaconcino devono essere da limpidi a leggermente opalescenti, da incolori a giallo chiaro.
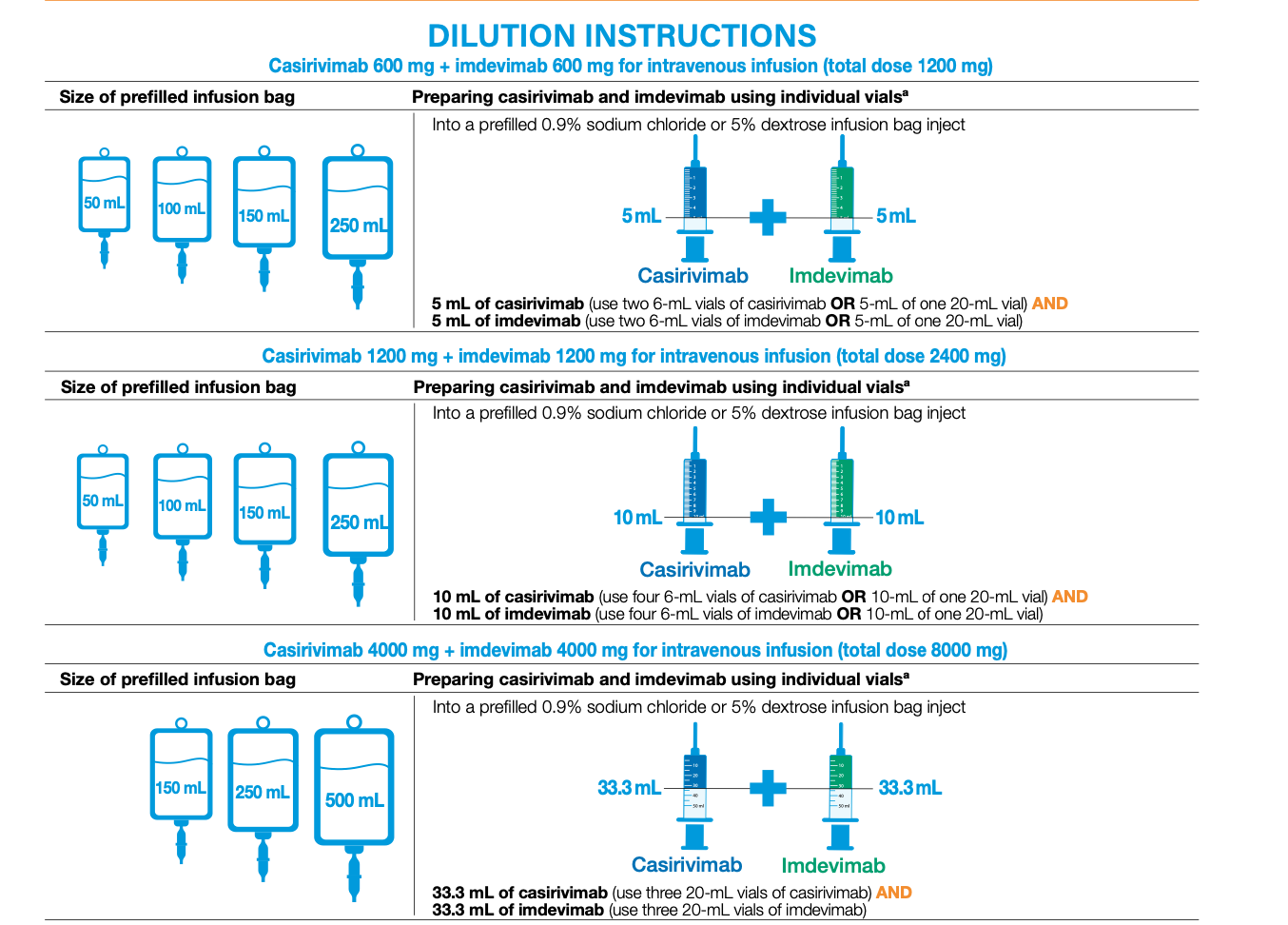
- Procurarsi una sacca endovenosa da 250 mL di cloruro di sodio allo 0,9% per preparazioni iniettabili. Non usare altri diluenti.
- Utilizzare una combinazione appropriata di nuove siringhe per prelevare 66,6 mL di cloruro di sodio allo 0,9% dalla sacca endovenosa ed eliminarli.
- Utilizzando nuove siringhe con nuovi aghi, prelevare un volume totale di 33,3 mL di casirivimab dai flaconcini di concentrato (utilizzare 3 flaconcini da 11,1 mL oppure 14 flaconcini da 2,5 mL).
- Aggiungere 33,3 mL di casirivimab alla sacca di cloruro di sodio allo 0,9%. Capovolgere delicatamente (NON agitare) la sacca endovenosa 10 volte per assicurarsi che la soluzione di casirivimab e la soluzione di cloruro di sodio allo 0,9% siano ben miscelate.
- Utilizzando nuove siringhe con nuovi aghi, prelevare un volume totale di 33,3 mL di imdevimab dai flaconcini di concentrato (utilizzare 3 flaconcini da 11,1 mL oppure 14 flaconcini da 2,5 mL).
- Aggiungere 33,3 mL di imdevimab alla sacca di cloruro di sodio allo 0,9% già contenente casirivimab. Capovolgere delicatamente (NON agitare) la sacca endovenosa 10 volte per garantire che i due anticorpi monoclonali e la soluzione di cloruro di sodio allo 0,9% siano ben miscelati. Chiudere la porta di ingresso della sacca per infusione endovenosa come da prassi locale.
- Questo prodotto è privo di conservanti, pertanto la soluzione per infusione diluita deve essere somministrata immediatamente.
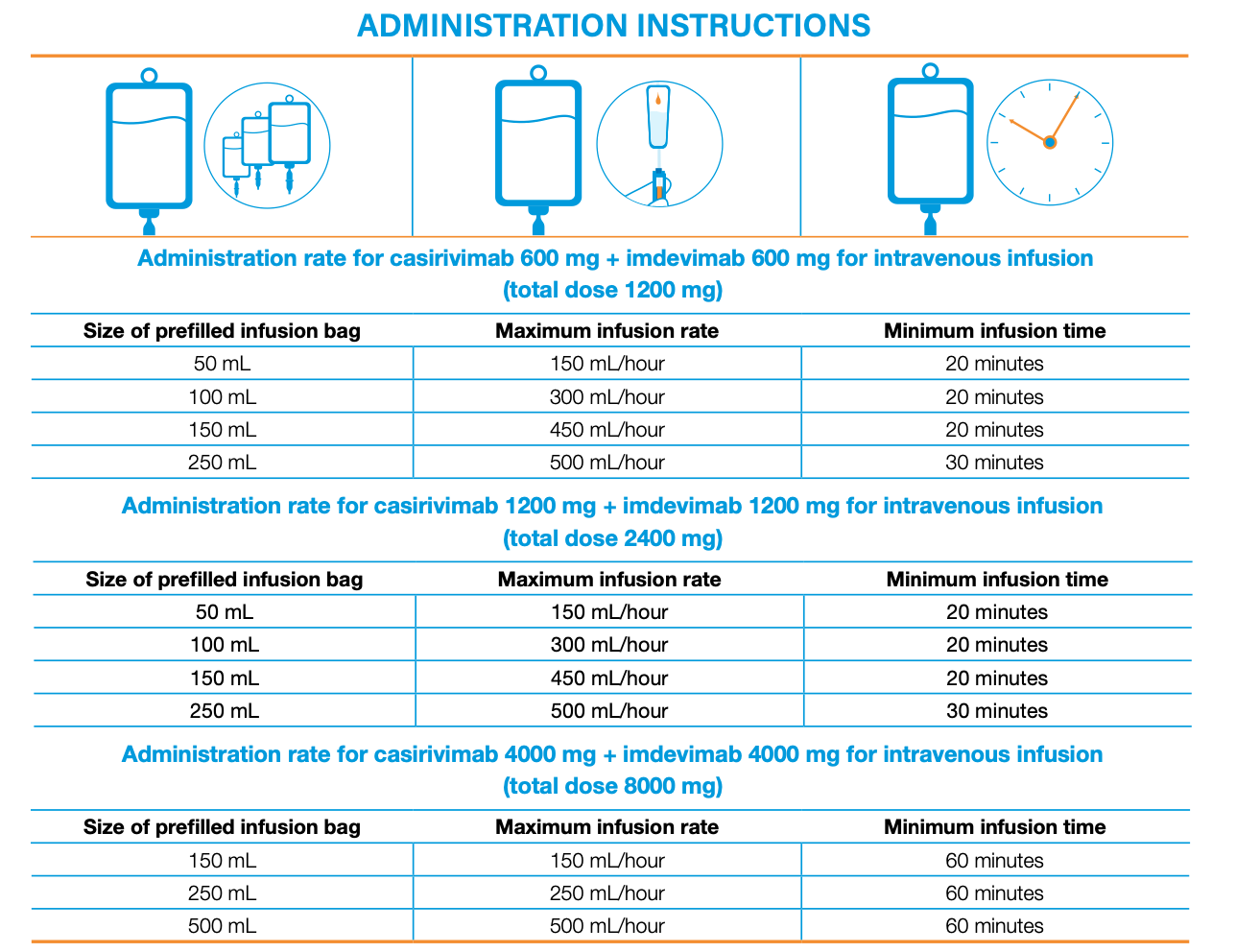
La soluzione va somministrata in un tempo minimo di 60 minuti, 250 ml/ora.
Se non eÌ€ possibile somministrarla immediatamente, conservare la soluzione diluita di casirivimab e imdevimab in frigorifero a una temperatura compresa tra 2 °C e 8 °C per non piuÌ€ di 36 ore oppure a temperatura ambiente fino a 25 °C per non piuÌ€ di 4 ore. Se la soluzione per infusione viene refrigerata, riportarla a temperatura ambiente attendendo circa 30 minuti prima della somministrazione.
Materiale necessario
Set per infusione in polivinilcloruro o poliuretano.
Filtro in polietersulfone in linea o aggiuntivo da 0,2 micron.
Istruzioni
- Attaccare il set per infusione alla sacca per infusione.
- Somministrare l'intera soluzione per infusione tramite pompa o per gravità
- NON somministrare la soluzione per infusione con un altro farmaco.
- Una volta completata l'infusione, lavare la linea con cloruro di sodio allo 0,9% o destrosio al 5%.
- Monitorare clinicamente il paziente durante l'infusione e peR 1 ora dopo l'infusione a intervalli di 15 minuti.
- Controllare la pressione sanguigna, la frequenza cardiaca, la saturazione di ossigeno e temperatura.
PREPARAZIONE E SOMMINISTRAZIONE DEI MONOCLONALI PER VIA SOTTOCUTANEA
- Le iniezioni sottocutanee (SC) di casirivimab e imdevimab devono essere somministrate indipendentemente e non mescolate.
- Prelevare la quantità appropriata di casirivimab e imdevimab in siringhe separate da 3 ml o 5 ml utilizzando aghi di calibro 21.
- Sostituire l’ago con cui abbiamo prelevato il farmaco con aghi da 25 a 27 per iniezione sottocutanea.
- Somministrare immediatamente il prodotto. Se non si è in grado di somministrare immediatamente, le siringhe possono essere conservate a temperatura ambiente per un massimo di 4 ore.
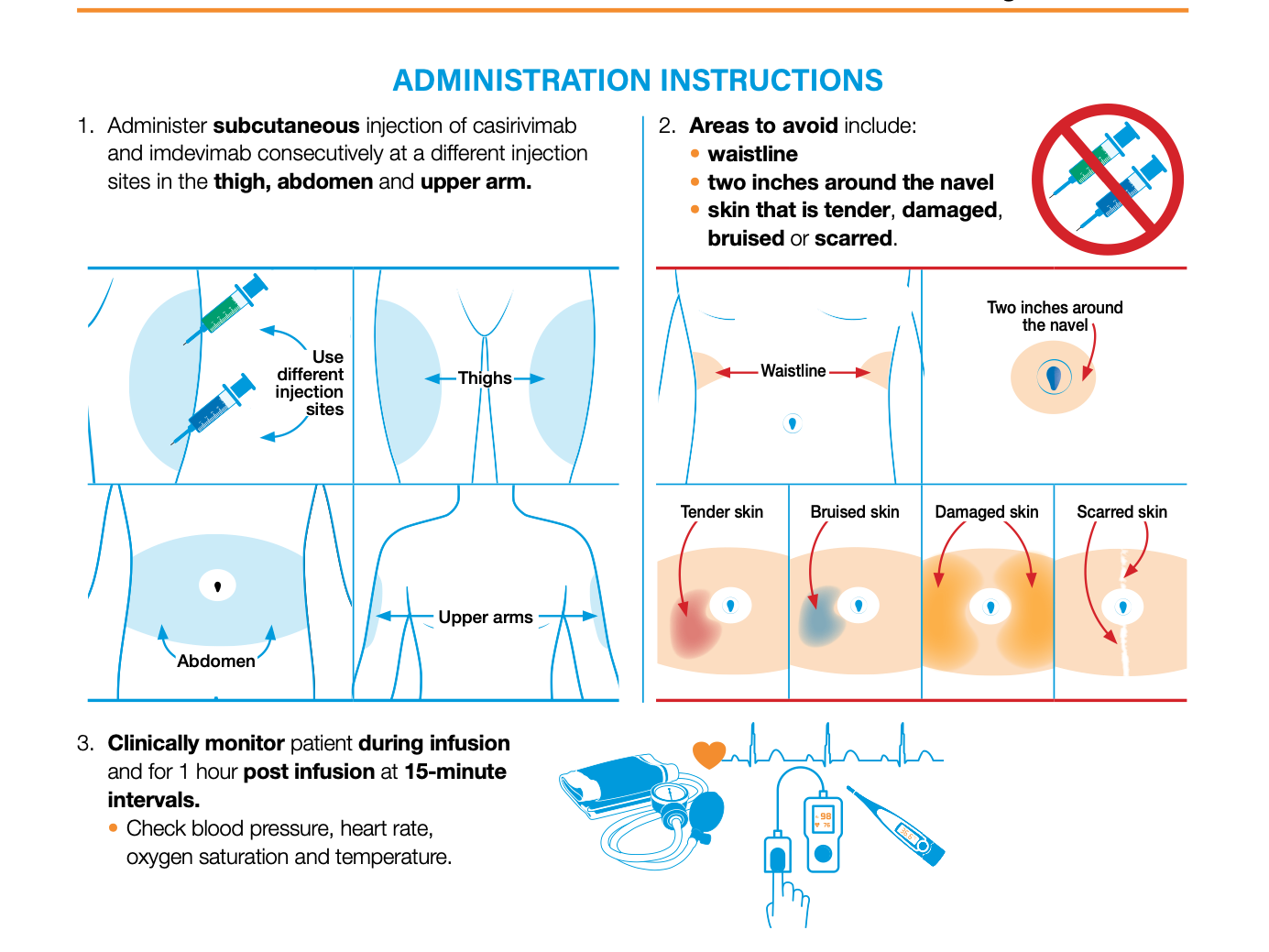
- Somministrare l'iniezione sottocutanea di casirivimab e imdevimab consecutivamente in siti di iniezione diversi, nella coscia, nell'addome e nella parte superiore del braccio.
- Le aree da evitare includono: • girovita, due pollici intorno all'ombelico, pelle danneggiata, contusa o sfregiata
- Monitorare clinicamente il paziente durante l'infusione e per 1 ora dopo l'infusione a intervalli di 15 minuti.
- Controllare la pressione sanguigna, la frequenza cardiaca, saturazione di ossigeno e temperatura.
Reazioni di ipersensibilità
Con casirivimab e imdevimab sono state segnalate gravi reazioni di ipersensibilità, inclusa anafilassi.
- Sono state segnalate reazioni di ipersensibilità verificatesi > 24 ore dopo la somministrazione di casirivimab e imdevimab.
- Se si verificano segni o sintomi di una reazione di ipersensibilità clinicamente significativa o anafilassi, interrompere immediatamente l'infusione e iniziare i farmaci appropriati, la terapia di supporto e la gestione delle vie aeree.
- Gravi reazioni allergiche possono causare gonfiore delle vie aeree e causare difficoltà respiratorie.
- Somministrare adrenalina per via intramuscolare in caso di ostruzione delle vie aeree, forte respiro sibilante o shock. Poiché l'adrenalina può svanire in pochi minuti, preparati a somministrare dosi aggiuntive.
- Assicurarsi che il paziente abbia una flebo per la somministrazione di liquidi per via endovenosa.
- Continuare a (ri)valutare le vie aeree e somministrare ossigeno secondo necessità.
- Se il paziente ha una grave anafilassi o non sta migliorando, prendere in considerazione il trasferimento a un livello di assistenza più elevato per un'ulteriore gestione.
Altre reazioni (da gravi a lievi) sono:
- Difficoltà respiratorie − Broncospasmo
- Ipotensione
- Angioedema
- Sincope
- Respirazione difficoltosa
- Battito cardiaco irregolare
- Ridotta ossigenazione
- Dolore o fastidio al torace − Ipertensione
- Brividi
- Febbre
- Diaforesi
- Vertigini
- Mal di testa
- Dolori muscolari
- Irritazione alla gola − Nausea
- Fatica
- Debolezza


 di
di